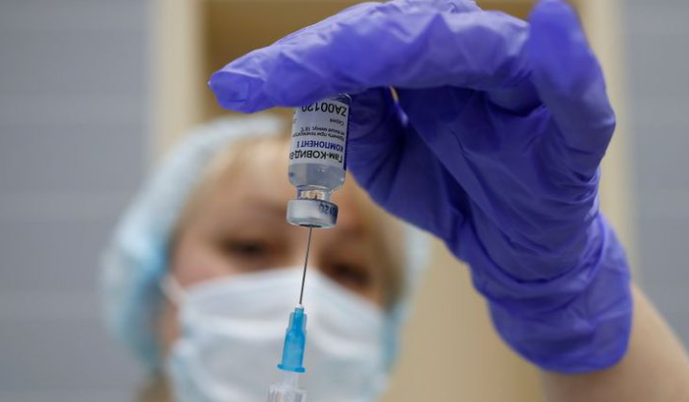
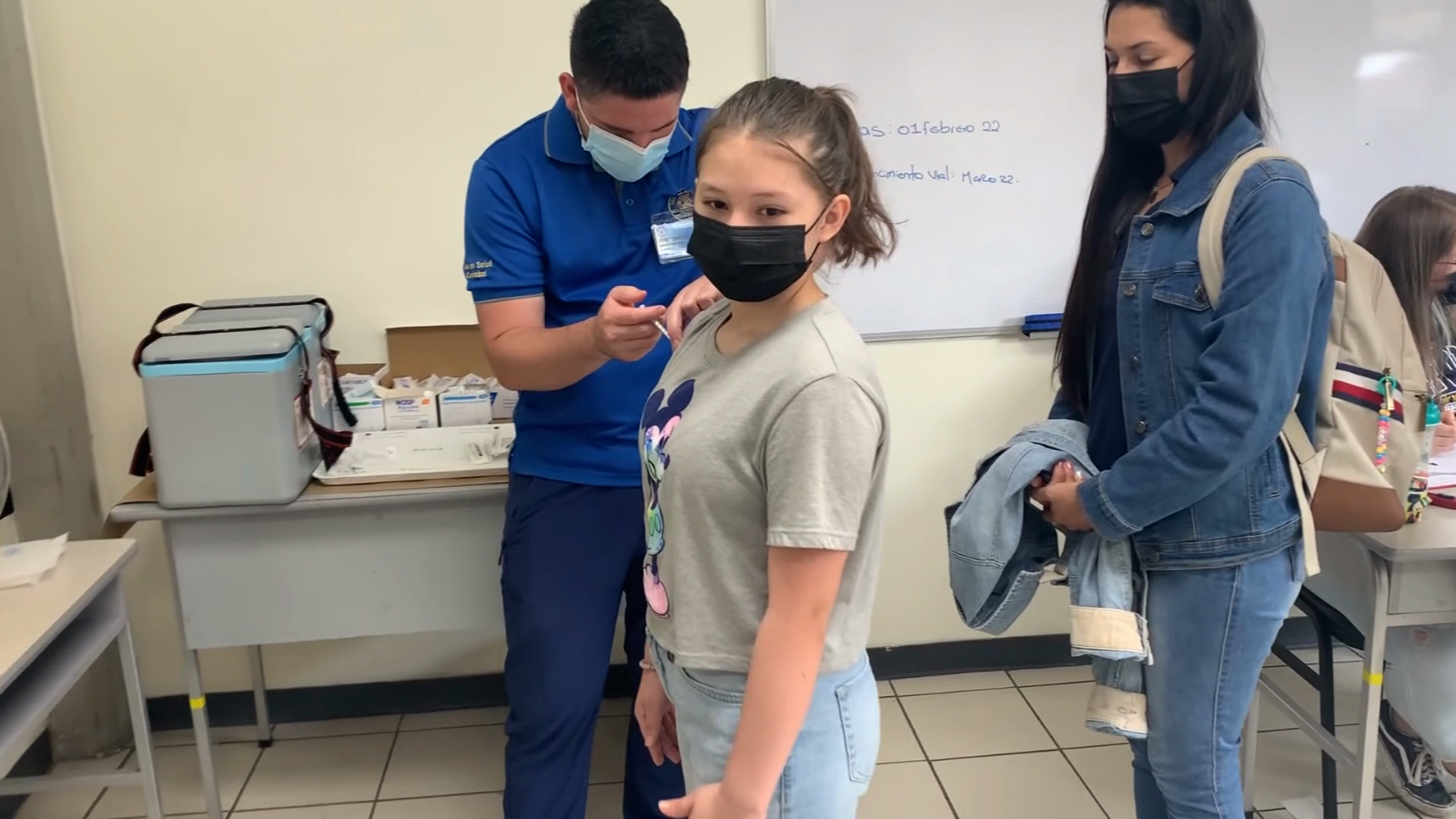
Sin agujas, más baratas y contra todas las cepas: cómo son las vacunas de segunda generación contra COVID-19
06 junio 21
Una verdadera revolución tecnológica dispuesta al servicio de la medicina estamos viviendo desde hace más de un año, cuando irrumpió en el mundo la pandemia por el nuevo coronavirus SARS-CoV-2 que generó la enfermedad COVID-19, la cual ya infectó a más de 173 millones de personas y provocó el fallecimiento de 3,7 millones de almas.
Si bien se desarrollaron todo tipo de mecanismos de ayuda sanitaria, tratamientos y drogas contra la nueva enfermedad, la herramienta que más elogios despertó y la única que puede terminar con esta pesadilla son las vacunas.
A casi un año y medio del surgimiento del virus en China, el mundo ya dispone de varias inoculaciones eficaces y seguras para combatir al patógeno y evitar que las personas sufran la enfermedad que genera en una forma grave.
Si bien las vacunas son muy buenas, varios laboratorios, universidades y compañías farmacéuticas en todo el mundo van por más y mejores soluciones a la ya existentes, pensando en desarrollar dosis que abarquen a las nuevas cepas de este coronavirus (polivalentes) y también a los otros dos mortales, como el SARS y el MERS. Vacunas que además sean más fáciles de producir, más baratas y también más simples de administrar con solo una dosis, almacenar y hasta de aplicar, pensando en inoculaciones inhalantes, o con un parche.Y por supuesto, que todas ellas sean eficaces y generen menos efectos secundarios.
“COVID-19 no será una pandemia para siempre, pero es probable que el virus que la causa sea ilimitado, como la gripe. ¿Tendremos que poner una vacuna mientras exista este virus en el mundo? Creo que la respuesta a esa pregunta es sí”, dijo en una reciente conferencia el doctor Paul Offit, director del Centro de Educación sobre Vacunas, profesor de pediatría en el Hospital de Niños de Filadelfia y co-creador de una de las vacunas más importantes que se dan actualmente como la del rotavirus. “Existe una larga historia en las vacunas de segunda generación que son muchas veces mejores que las vacunas de primera generación. Así son las cosas”, afirmó Scott Roberts, director científico de Altimmune, una empresa de biotecnología con sede en Gaithersburg, Maryland, que está desarrollando el sistema para que la vacuna sea administrada por inhalación.
Ninguna de estas vacunas COVID-19 de segunda generación estará lista, al menos hasta 2022. Potencialmente, cada una de las casi 8 mil millones de personas en la Tierra necesitará una o dos dosis iniciales y posiblemente refuerzos, por lo que hay suficiente espacio para diferentes enfoques, dicen los expertos. “Profundidad y amplitud” es lo que el vacunólogo, farmacéutico y líder de salud pública John Grabenstein dijo que quería de una vacuna contra COVID-19 de segunda generación, ya que espera la ansiada protección contra diversas variantes y enfermedades respiratorias e idealmente una década o más entre tomas, como ocurre con la vacuna de la fiebre amarilla.
La Administración de Alimentos y Medicinas de Estados Unidos (FDA) ya les pidió a las compañías farmacéuticas que adapten su tecnología para desarrollar vacunas que enfrenten las nuevas y las futuras variantes del SARS-CoV-2. Para ello, por ejemplo, los laboratorios Moderna y Pfizer que tienen en el mercado vacunas seguras y eficaces aprobadas y administradas a millones de personas, ya están desarrollando nuevas inoculaciones llamadas de segunda generación.
Moderna, que como sabemos, desarrolló su vacuna en colaboración con el Instituto Nacional de Enfermedades Infecciosas y Alergias de Estados Unidos ha anunciado que está trabajando en tres frentes respecto a una nueva generación de vacunas contra el COVID-19. El primero es que ha desarrollado ya una nueva vacuna dirigida específicamente contra la variante sudafricana, bautizada como mRNA 1273.351, y las primeras dosis fueron enviadas al Instituto Nacional de Enfermedades Infecciosas y Alergias para su respectiva evaluación. La idea es usar esta nueva vacuna como un refuerzo en quienes han recibido las primeras dos dosis de la vacuna de primera generación. También, como la nueva vacuna para quienes no han sido vacunados previamente o que no han tenido la enfermedad.
Recordemos que, al usar un código genético del nuevo coronavirus para elaborar su vacuna de ARN mensajero, a los investigadores les basta leer el nuevo genoma de la variante -al igual que uno lee un documento en la computadora- para detectar los cambios producidos en la variante y elaborar la nueva molécula de ARN mensajero.
La segunda estrategia de Moderna es preparar una vacuna que -al igual de lo que sucede con la gripe- sea polivalente. Es decir, que contenga una mezcla de las vacunas de primera y segunda generación, para cubrir las nuevas variantes. Recordemos que, al vacunarnos cada año contra la gripe, recibimos vacunas que son polivalentes, compuestas por tres virus de la gripe, escogidos por ser los que más casos causaron en el invierno del hemisferio opuesto al que se quiere vacunar. Por último, Moderna está estudiando una vacuna que usa menos de los 100 microgramos de ARN mensajero de la que tienen sus actuales vacunas.La idea es averiguar si estas vacunas con dosis más bajas puedan despertar también la inmunidad en los voluntarios, algunos de los cuales, ya están recibiendo estas dosis de refuerzo con menor cantidad de ARNm.
Con respecto a Pfizer, la compañía anunció también algunos cambios en su estrategia para enfrentar a la pandemia. En primer lugar, está también probando -al igual que Moderna- si una tercera dosis de su vacuna podría funcionar como un refuerzo capaz de neutralizar las variantes. Para eso, han reclutado a 144 participantes de su ensayo de fase 1 que se hizo en Estados Unidos en la primera mitad del año 2020, y que incluye a algunos voluntarios mayores de 85 años.
El estudio evaluará la seguridad y la respuesta inmunológica que produce una dosis de refuerzo en los voluntarios, los que, al haber recibido las primeras dosis en la primera mitad del año 2020, darán una mejor idea de lo que es aplicar un refuerzo 6 a 12 meses después de las primeras. La dosis del refuerzo sería idéntica a la actualmente autorizada, es decir 30 microgramos.
En segundo lugar, Pfizer y BioNTech están planeando desarrollar también una vacuna de segunda generación, y están en conversaciones para enrolar nuevos voluntarios en estudios de fase 1 y fase 2. Las acciones de los laboratorios mencionados van de acuerdo con la recomendación de la FDA, de que por ahora -y con cargo a discutir los detalles en el futuro- las nuevas vacunas no tengan que pasar por los largos estudios de fase 1, 2 y 3, sino que demuestren la capacidad que tienen de estimular al sistema de defensa en estudios en cientos de personas que no hayan sido vacunadas previamente, así como estudiar el efecto de las nuevas vacunas como dosis de refuerzo, en las personas previamente vacunadas.
Además de la farmecéuticas exitosas que tienen una vacuna contra COVID-19 aprobada, hay otras empresas y hasta universidades que están en la última etapa de desarrollo y estudios clínicos de sus nuevas vacunas más baratas, fáciles de producir y polivalentes, es decir que sirven para las nuevas variantes del coronavirus. Infobae repasó las 18 vacunas de segunda generación que próximamente saldrán al mercado.
1) Novavax es una empresa de biotecnología con sede en Gaithersburg, Maryland, EEUU, que está trabajando en su vacuna NVX-CoV2373 de proteína que involucra un portador de nanopartículas para ayudar mejor a la entrega y absorción por las células. La vacuna se administra en dos dosis, con 21 días de diferencia. El 11 de marzo, Novavax anunció que un análisis final de sus ensayos clínicos de fase tres en el Reino Unido muestra que su vacuna tiene una efectividad del 96,4 por ciento en la prevención de COVID-19. También anunció los hallazgos de su ensayo clínico de fase 2b en Sudáfrica, que mostró que la vacuna tenía solo un 48,6 por ciento de efectividad contra las cepas que circulaban allí. Ambos ensayos mostraron que la vacuna es 100 por ciento efectiva para prevenir casos graves de la enfermedad.
2) Sanofi-GSK, laempresa biofarmacéutica mundial está desarrollando una vacuna de proteína recombinante con adyuvante que está siendo estudiada en un estudio clínico de fase III. El estudio probará la seguridad y eficacia de la vacuna en 35.000 voluntarios de 18 años o más en los EEUU, Asia, África y América Latina. La amplia gama geográfica del estudio permitirá a las empresas evaluar la eficacia de la vacuna contra las variantes del virus que circulan por el mundo.
3) E. Biológico Limitado es una compañía farmacéutica y de vacunas de la India, que en asociación con el Baylor College of Medicine están fabricando una vacuna de subunidades a base de proteínas que requiere dos dosis administradas con 28 días de diferencia. El 26 de abril, las empresas anunciaron que habían recibido la aprobación para lanzar un ensayo clínico de fase III que evaluará su eficacia y seguridad entre más de 1.200 voluntarios de entre 18 y 80 años en 15 ciudades de la India.
4) Valneva SE, un laboratorio francés, trabaja con la vacuna VLA2001, de virus inactivado, con adyuvante, y dos dosis administradas con tres semanas de diferencia. El 21 de abril, Valneva anunció el lanzamiento de ensayos clínicos de fase III para estudiar la seguridad y eficacia de su vacuna COVID-19 en comparación con la vacuna de AstraZeneca. Aproximadamente 4.000 voluntarios recibirán dos dosis de cualquiera de las vacunas para determinar la respuesta inmunitaria de cada una. Valneva dice que espera solicitar la aprobación regulatoria hacia fin del 2021.
5) Productos biológicos de Shenzhen Kangtai es una empresa farmacéutica con sede en China que ya cuenta con la aprobación de las autoridades chinas de salud para aplicar una vacuna inactivada que requiere dos dosis administradas con 28 días de diferencia. Los ensayos clínicos de fase tres de Kangtai están en marcha , probando la seguridad y eficacia de la vacuna entre 28.000 adultos mayores de 18 años.
6) Medicago es una empresa canadiense de biotecnología, en asociación con la empresa farmacéutica multinacional británica GlaxoSmithKline que trabaja en la vacuna CoVL recombinante de origen vegetal con un adyuvante que requiere dos dosis administradas con 21 días de diferencia. El 16 de marzo, Medicago y GlaxoSmithKline anunciaron que su vacuna había entrado en ensayos clínicos de fase III para estudiar su seguridad y eficacia en hasta 30.000 voluntarios en 10 países, incluidos Canadá y EEUU. En noviembre de 2020, las empresas dijeron que su fase uno de los ensayos clínicos mostró que la vacuna produjo respuestas de anticuerpos y de células T sin que se informaran eventos adversos graves.
7) Bharat Biotech, una empresa de biotecnología india, en colaboración con el Consejo Indio de Investigación Médica y el Instituto Nacional de Virología, desarrolló la vacuna COVAXIN inactivada, ya aprobada por India, que requiere dos dosis que se administran con 28 días de diferencia. En su ensayo de fase III mostró que su vacuna es 81 por ciento efectiva en la protección contra COVID-19 después de la segunda dosis. Otro estudio preliminar también indicó que la vacuna produce anticuerpos que pueden neutralizar la variante del virus que se originó en el Reino Unido.
8) El Instituto Finlay de Vacunas desarrolló en Cuba Soberana-02, una vacuna conjugada que usa parte de la proteína del pico del virus. El gobierno cubano no ha publicado ningún dato de los ensayos en etapa inicial, pero dijo que el ensayo de fase tres se está llevando a cabo en La Habana entre 44.000 voluntarios.
9) El Centro de Chumakov de Rusia desarrollo CoviVac, una vacuna inactivada administrada en dos dosis, con 14 días de diferencia que logró el 20 de febrero la aprobación para su uso, aunque aún no han comenzado los ensayos clínicos en etapa tardía para probar su seguridad y eficacia.
10) El Instituto de Investigación Infantil Murdoch, desarrolló BRACE de Bacillus Calmette-Guerin es eEl instituto de investigación en salud infantil más grande de Australia, que, en colaboración con la Universidad de Melbourne está trabajando en vacunas contra COVID-19 en base a su exitosa vacuna Bacillus Calmette-Guerin (BCG) que se ha utilizado para prevenir la tuberculosis al exponer a los pacientes a una pequeña dosis de bacterias vivas. A lo largo de los años, ha surgido evidencia de que esta vacuna puede estimular el sistema inmunológico y ayudar al cuerpo a combatir otras enfermedades también. El 10 de noviembre, un estudio de EE. UU. Publicado en el Journal of Clinical Investigation encontró que entre 6,201 trabajadores de la salud en Los Ángeles, aquellos que habían recibido previamente la vacuna BCG informaron síntomas de COVID-19 con menos frecuencia que aquellos que no lo habían hecho
11) El Instituto de Vector de Rusia lleva adelante EpiVacCorona, una vacuna de proteínas, que utiliza pequeños fragmentos de antígenos virales llamados péptidos para producir una respuesta inmune.
12) CureVac, la empresa biofarmacéutica alemana en asociación con la gigante Bayer está detrás de CVnCoV, una vacuna de ARNm que se administra en dos dosis tomadas con 28 días de diferencia. La segunda versión de la vacuna CureVac provocará una respuesta inmune más alta que la primera a una dosis más baja y no habrá problemas con el almacenamiento en frío de otras vacunas de ARNm, dijo Mariola Fotin-Mlecek, director tecnológico jefe de la empresa.
13) Zydus Cadila es otra empresa farmacéutica india detrás de ZyCoV-D, una vacuna basada en ADN que se administra mediante un parche cutáneo. El 3 de enero, Zydus Cadila anunció que había recibido la aprobación de los reguladores indios para lanzar un ensayo de fase tres que prueba la seguridad y eficacia de su vacuna en unos 30.000 voluntarios.
14) Anhui Zhifei, una empresa biofarmacéutica china, en asociación con el Instituto de Microbiología de la Academia de Ciencias de China desarrolló ZF2001, una vacuna de subunidad que utiliza partes de proteína de un patógeno para desencadenar una respuesta inmunitaria. En noviembre, los funcionarios de salud chinos anunciaron el lanzamiento de ensayos de fase tres para la vacuna Anhui Zhifei. Se espera que los ensayos, que reclutarán a 29.000 voluntarios de 18 años o más, se realicen en China, Indonesia, Pakistán y Ecuador.
15) El Instituto de Investigación de Problemas de Seguridad Biológica en Kazajstán elaboró QazCovid-in, una vacuna inactivada que logró que le otorgaran un registro temporal de nueve meses, a pesar de la falta de datos de sus ensayos de fase tres en curso.
16) El Instituto de Biología Médica de la Academia China de Ciencias Médicas también está desarrollando su vacuna inactivada que requiere dos dosis tomadas con 14 días de diferencia. En diciembre, los investigadores lanzaron ensayos clínicos de fase tres para probar la eficacia y seguridad de la vacuna en 34.020 participantes en Malasia y Brasil.
17) Gritstone Oncology es una empresa de biotecnología en etapa clínica con sede en EEUU, con el apoyo de los departamentos de los NIH y la Fundación Bill & Melinda Gates. Los investigadores la Escuela de Medicina de la Universidad de Washington (UW) están comenzando a inscribir voluntarios para un ensayo clínico que evalúa una vacuna COVID-19 de segunda generación llamada Coral. El estudio multicéntrico de Fase 1 examinará la seguridad, la tolerabilidad y la respuesta inmune para diferentes dosis de un régimen de vacuna COVID-19 en investigación de dos partes. La segunda etapa del estudio incluirá vacunas con múltiples proteínas SARS-CoV-2, además de los componentes de la proteína Spike que se utilizan en las vacunas COVID-19 actuales administradas bajo la Autorización de uso de emergencia de la FDA.
18) En Argentina, investigadores de la Fundación Instituto Leloir (FIL) y del Conicet, junto con la compañía biotecnológica Vaxinz están tras el desarrollo de una vacuna de segunda generación contra el coronavirus que ya indujo una respuesta inmune muy potente en laboratorio. La misma, utiliza la plataforma de vector viral no replicante, es decir que toma un virus que no produzca efectos graves de salud, lo modifica genéticamente para que no se replique en el organismo y le “introduce” una parte del virus contra el cual se quiere inocular, en este caso se trata de la proteína Spike del coronavirus. Parte de un adenovirus humano que causa un resfrío común, el adenovirus 5 (similar al de la segunda dosis de Sputnik V), al cual se le hicieron modificaciones con partes de otros adenovirus humanos, por eso es un híbrido.