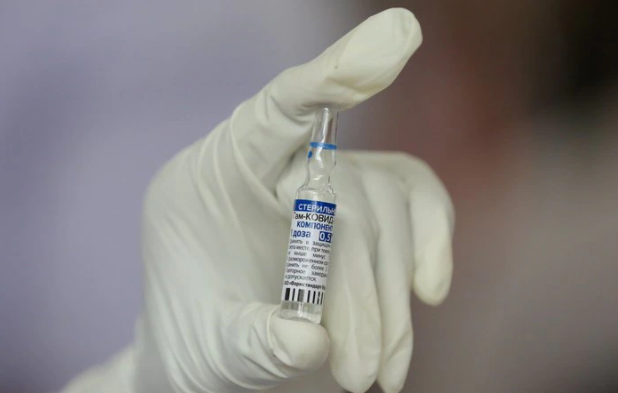
Brasil rechazó la solicitud para evaluar el uso de emergencia de la vacuna rusa Sputnik V
17 enero 21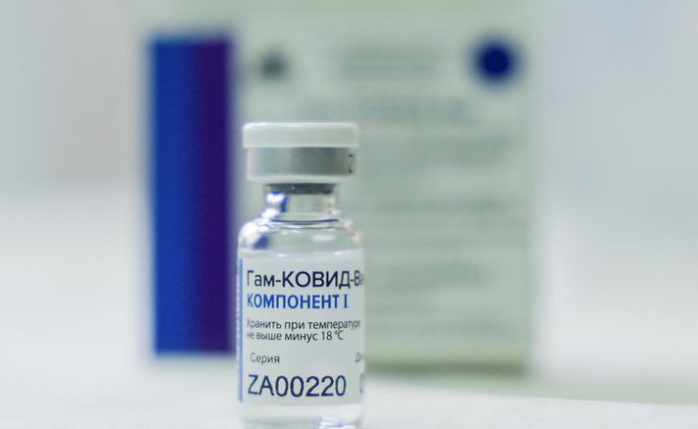
La Agencia Nacional de Vigilancia Sanitaria de Brasil (Anvisa) rechazó la solicitud de autorización de emergencia de la vacuna rusa Sputnik V, según un comunicado publicado por el organismo.
Según detalla el texto, la razón es que los documentos no presentaban “requisitos mínimos de presentación y análisis, y las cuestiones relacionadas con las buenas prácticas de fabricación”. La solicitud -finalmente vetada- para el uso de emergencia de 10 millones de dosis de la vacuna rusa fue presentada por la compañía farmacéutica União Química el viernes 15 de enero.
En el comunicado, Anvisa citó la falta de estudios clínicos sobre la vacuna de fase tres. La semana pasada, la agencia determinó como uno de los criterios para la solicitud y el uso de emergencia de la vacuna que el laboratorio lleve a cabo la fase tres de los estudios – la fase de análisis clínico – en Brasil.
Hasta ahora, el desarrollo ruso no ha iniciado esta etapa del proceso en territorio brasileño. El organismo aclara que no basta con que la solicitud de autorización de la fase tres del ensayo clínico se presente para uso de emergencia. Es necesario que esos estudios estén en curso en el país.
Según el organismo, la solicitud de autorización de uso de emergencia “debe incluir estrategias que el solicitante aplicará para garantizar que los ensayos clínicos en curso de la vacuna puedan evaluar la seguridad y la eficacia a largo plazo”.
União Química solicitó formalmente a Anvisa, a finales de diciembre, la autorización para comenzar la fase tres de las pruebas del Sputnik, pero la solicitud aún no ha sido aprobada por la agencia porque se identificó que “faltan documentos”. Así pues, el 4 de enero, el Organismo pidió al laboratorio que presentara la información que faltaba y la complementaria. El 6 de enero, la compañía respondió que tan pronto como pueda cumplir con el requisito lo completaría. Pero, asegura el comunicado, “hasta ahora, Anvisa está esperando que la empresa cumpla con el requisito de completar el análisis de la solicitud de estudio”.
Por su parte, el Fondo Ruso de Inversión Directa, desarollador de la Sputnik V, respondió que la información adicional solicitada por Brasil “será proporcionada en breve” y manifestó su confianza en que con ella se autorizará su producción en ese país.
La Sputnik V fue aprobada en Argentina, Venezuela, Bolivia, México , Paraguay, Egipto, Corea del Sur, India, Nepal, Bielorrusia, Kazajstán, Uzbekistán y Argelia.
La Anvisa decide este domingo si autoriza el uso en el país, por condiciones de emergencia, de las dos únicas vacunas cuyos laboratorios sí completaron sus procesos para registrar sus productos: la farmacéutica china Sinovac y la desarrollada conjuntamente por el laboratorio británico AstraZeneca y la Universidad de Oxford.
Cinco directores de Anvisa participarán en esta reunión de forma excepcional, que está prevista que comience a las 10 de la mañana y durará cinco horas. En esta evaluación final, si al menos tres directores votan a favor del uso de emergencia, las vacunas pueden ser usadas en Brasil, y el gobierno puede comenzar el Plan Nacional de Inmunización.
El Instituto Butantan, vinculado al Gobierno del estado de Sao Paulo y que trabaja desde hace varios meses en el desarrollo de la vacuna china, y la Fundación Fiocruz, que hace lo propio con la de AstraZeneca y la universidad británica de Oxford, realizaron pruebas de sus antivirus en miles de voluntarios.
Con un 50,4 % y un 70 % en promedio de eficacia, las vacunas de Sinovac y AstraZeneca, respectivamente, son las apuestas firmes de Brasil para reducir el número de hospitalizaciones y muertes por covid-19, después de un aumento disparado de los casos en plena segunda ola de la pandemia sin nunca haber controlado la primera.